Dalla ricerca di base alla pratica clinica: definire il futuro delle strategie terapeutiche nel microcitoma
L’immunoterapia e i progressi in biologia molecolare e immunoncologia offrono nuove speranze ai pazienti con SCLC. All’interno del progetto Science Clinic Life Collaboration, realizzato con il contributo non condizionante di Roche, il gruppo di lavoro “Ricerca” ha analizzato i progressi nell’immunoterapia e nelle tecniche innovative per il trattamento del SCLC.
Emilio Bria1, Dario Sangiolo2, Stefano Indraccolo3, Federica Biello4, Alessio Cortellini5, Manolo D’Arcangelo6, Vincenzo di Noia7, Stefano Frega8, Vito Longo9, Giuseppe Lo Russo10, Francesca Mazzoni11, Agnese Montanino12, Floriana Morgillo13
1Oncologia medica, Fondazione Policlinico Universitario A. Gemelli, IRCCS Università Cattolica del Sacro Cuore Policlinico Gemelli, Roma, 2Dipartimento di Oncologia, Università degli Studi di Torino, Istituto di Candiolo FPO-IRCCS, Torino, 3UOSD Oncologia di Base Sperimentale e Traslazionale, Istituto Oncologico Veneto IRCCS, Padova, 4Dipartimento Medico Specialistico ed Oncologico, AOU Ospedale Maggiore della Carità, Novara. 5Oncologia Medica, Fondazione Policlinico Universitario Campus Bio-medico Roma, 6Oncologia Medica, AUSL Romagna, Ospedale Santa Maria delle Croci, Ravenna, 7Oncologia Medica, IFO - Istituto Nazionale Tumori Regina Elena, Roma, 8Oncologia Medica, Istituto Oncologico Veneto - IOV, IRCCS, Padova, 9Oncologia Medica Toracica, Istituto Oncologico Giovanni Paolo II, Bari, 10Unità Oncologia Toracica - Oncologia Medica 1, Fondazione IRCCS Istituto Nazionale dei Tumori - INT, Milano, 11SOD Oncologia Medica, AOUC Azienda Ospedaliero-Universitaria Careggi, Firenze, 12Oncologia Medica, Istituto Nazionale Tumori IRCCS Pascale, Napoli, 13Oncologia Medica, Dipartimento di Medicina di Precisione dell’Università degli Studi della Campania “L. Vanvitelli”. Napoli
Il carcinoma polmonare a piccole cellule (Small Cell Lung Cancer, SCLC) è il sottotipo istologico più aggressivo di cancro al polmone e rappresenta circa il 13-15% di tutti i tumori polmonari.1 La natura recalcitrante del SCLC è evidenziata dalla rapida progressione della malattia accompagnata da manifestazioni metastatiche precoci.2 Più di due terzi dei pazienti presentano già una malattia avanzata al momento della diagnosi.3 Inizialmente, il SCLC è altamente sensibile alla chemioterapia con o senza radioterapia, mostrando tassi di risposta superiori al 60%; tuttavia, quasi tutti i pazienti sviluppano recidive e resistenza al trattamento.4 L’introduzione delle terapie con inibitori dei checkpoint immunitari (ICI) ha ampliato le opzioni terapeutiche disponibili per il SCLC; ciononostante, il microcitoma è una patologia per la quale al momento non esistono predittori di risposta per l’unica categoria di farmaci che sembra offrire un miglioramento prognostico.
Negli ultimi anni, la ricerca sul microcitoma ha guadagnato terreno, promettendo di aprire nuovi scenari nel trattamento di questa patologia. Innovazioni significative nella comprensione dei meccanismi molecolari alla base della tumorigenesi del SCLC hanno portato all’identificazione di potenziali nuovi bersagli terapeutici e marcatori prognostici. In particolare, lo studio avanzato del microambiente tumorale (TME), l’impiego di tecniche di sequenziamento di nuova generazione e l’analisi di biomarcatori attraverso la biopsia liquida hanno rivelato complessità e vulnerabilità precedentemente inesplorate.
All’interno del progetto Science Clinic Life Collaboration, realizzato con il supporto non condizionante di Roche, il gruppo di lavoro dedicato alla “Ricerca” si è posto come obiettivo quello di esaminare come le ultime scoperte nella comprensione dei meccanismi alla base del microcitoma possano essere tradotte in strategie terapeutiche innovative. Nel corso del dibattito si è discusso di immunoterapia e nuovi bersagli terapeutici. Sono state inoltre esplorate le implicazioni di strategie combinate che integrano approcci tradizionali e nuove modalità di trattamento, nella speranza di superare la resistenza al trattamento e migliorare la sopravvivenza dei pazienti affetti da microcitoma.
Attraverso l’analisi di studi clinici recenti e dati sperimentali, si è fatta una panoramica degli avanzamenti della ricerca sul microcitoma, evidenziando come questi progressi potrebbero in futuro influenzare la pratica clinica e offrire speranza ai pazienti affetti da questa devastante malattia. Perseguendo questo scopo, il gruppo di lavoro ha offerto un’analisi sulle prospettive future della ricerca e sull’impatto potenziale delle nuove scoperte nella gestione del microcitoma. La struttura del progetto e dell’attività svolta dal gruppo di lavoro “Ricerca”, che nello specifico ha portato alla realizzazione di questo manoscritto, è riportata in figura 1.
FIGURA 1. Struttura del progetto Science Clinic Life Collaboration e metodologia applicata al gruppo di lavoro “Ricerca”.

Durante il workshop sono stati esaminati in dettaglio alcuni argomenti di particolare rilevanza nel campo della ricerca oncologica sul SCLC. Le discussioni su questi argomenti e gli spunti emersi sono illustrati nelle sezioni successive.
I nuovi standard di cura per la terapia di prima linea del carcinoma polmonare a piccole cellule in stadio esteso (ES-SCLC) si basano sui risultati positivi di numerosi studi controllati randomizzati (RCT) che hanno dimostrato la superiorità dell’aggiunta di ICI alla chemioterapia standard a base di platino.5-7 Tuttavia, un beneficio prolungato sembra evidente solo per un gruppo selezionato di pazienti.7 Fino ad ora sono stati studiati diversi biomarcatori predittivi (figura 2), ma l’identificazione prospettica dei pazienti che potrebbero beneficiare maggiormente di un trattamento con ICI rimane una sfida nel campo del SCLC.7
FIGURA 2. Biomarcatori di beneficio per l’immunoterapia nei pazienti con ES-SCLC (modificata e tradotta da Lorenzi et al. 2024).7
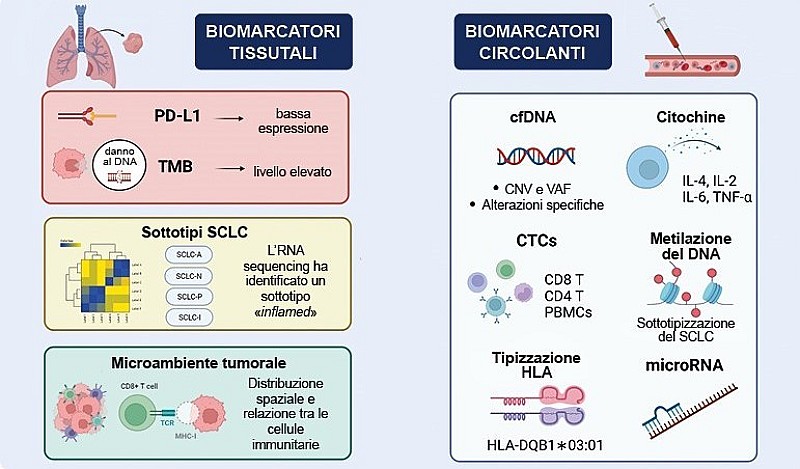
Legenda: TMB, carico mutazionale del tumore; PBMCs, cellule mononucleate del sangue periferico; HLA, antigene leucocitario umano
Biopsia liquida e trascrittomi nel SCLC: prospettive attuali e direzioni future
Data la complessa eterogeneità intra- e inter-tumorale nei SCLC, i campioni ottenuti da una sola biopsia possono non riflettere adeguatamente il profilo molecolare complessivo della malattia. Questa problematica è esacerbata dall’eterogeneità temporale, che si riferisce alla capacità del SCLC di evolversi e modificarsi in risposta alle terapie. La vera portata di questo fenomeno potrebbe essere osservata solo con biopsie ripetute nel tempo, una pratica poco realizzabile nei tumori polmonari. Inoltre, la disponibilità di tessuto per la ricerca traslazionale è limitata a causa della bassa percentuale di pazienti con SCLC che si sottopongono a interventi chirurgici. Tuttavia, recenti progressi nelle tecniche di biopsia liquida, che utilizzano plasma e altri fluidi biologici, offrono un’alternativa promettente per una valutazione più dinamica e meno invasiva dello stato del tumore.7 In questo contesto, la biopsia liquida, che include l’analisi del DNA circolante libero (cfDNA) e delle cellule tumorali circolanti (CTC), emerge come una tecnica promettente per il monitoraggio in tempo reale della malattia, offrendo una finestra sul profilo molecolare del tumore e fornendo informazioni diagnostiche e prognostiche prima del trattamento, durante il trattamento e nel corso della progressione della malattia.8
Gli studi sulle CTC hanno fondamento nel fatto che le CTC possono essere rilevate e monitorate serialmente nella maggior parte dei pazienti con SCLC.9 Le CTC del SCLC hanno dimostrato una sensibilità alla chemioterapia quando presenti come singole cellule; tuttavia, i tumori che recidivano dopo il trattamento iniziale tendono a manifestare una resistenza diffusa ai farmaci. Di conseguenza, una riduzione significativa delle CTC non implica necessariamente un’efficacia del trattamento sulle lesioni primarie.10
Gli studi di cfDNA si basano sulle tecnologie NGS e sui successi ottenuti in ambito di NSCLC.11-13
Attualmente sono disponibili pochi dati sul ruolo predittivo della biopsia liquida nel ES-SCLC trattato con ICI. Infatti, gli studi che esplorano il ruolo del cfDNA nel monitoraggio longitudinale della malattia includono generalmente un numero limitato di pazienti trattati solo con chemioterapia e sono volti a identificare il ruolo prognostico. I risultati suggeriscono un’associazione tra il livello quantitativo di cfDNA e l’esito, in particolare la sopravvivenza globale (OS). Inoltre, specifiche alterazioni sembrano essere associate alla chemiosensibilità.7 Oltre all’analisi quantitativa del cfDNA, sono state indagate anche le alterazioni genetiche qualitative del cfDNA, riscontrando, in una popolazione eterogenea di pazienti con SCLC, alcune aberrazioni genomiche (SETBP1, PBRM1, ATRX, EP300, ATM, PIK3CA/G o NOTCH1) quali potenziali biomarcatori dell’efficacia del trattamento e della prognosi della malattia.7 Clinici ed esperti del progetto Science Clinic Life Collaboration hanno messo in evidenza come, nel nuovo panorama terapeutico del SCLC, il cfDNA potrebbe consentire di monitorare la risposta al trattamento con maggiore precisione e tempestività rispetto alle tecniche di imaging convenzionali. Attraverso l’identificazione di mutazioni o variazioni genetiche del tumore durante il trattamento, il cfDNA fornisce una visione “istantanea” e aggiornata dello stato oncologico. Questo potrebbe consentire una valutazione dettagliata dell’efficacia terapeutica e una personalizzazione delle cure basata sull’evoluzione molecolare del tumore nel singolo paziente. L’analisi del cfDNA potrebbe consentire agli oncologi di adattare i protocolli terapeutici in risposta ai cambiamenti molecolari dinamici osservati, ed eventualmente indirizzare in maniera tempestiva i pazienti non responsivi alle terapie standard verso studi clinici appropriati, prima che il loro stato clinico precluda ulteriori opzioni terapeutiche.
Nonostante il notevole potenziale diagnostico e predittivo, la diffusione di questo test nel contesto clinico rimane un obiettivo lontano. Le principali barriere alla sua adozione su larga scala includono le difficoltà di accesso alla diagnostica avanzata e le sfide economiche legate ai costi delle tecnologie impiegate. Ciononostante, clinici ed esperti evidenziano che la biopsia liquida rappresenta un ambito di grande interesse sottolineando la necessità di un impegno continuo nella ricerca per correlare la risposta molecolare del tumore con la risposta clinica del paziente. Una particolare attenzione va rivolta allo studio dello stato di metilazione del cfDNA, alla trascrittomica e all’integrazione del dosaggio delle mutazioni e delle aberrazioni cromosomiche. Inoltre, è fondamentale valutare i pazienti tra il termine della chemioterapia e l’inizio dell’immunoterapia per determinare chi trarrà beneficio dall’immunoterapia dopo i cicli di induzione. Questo intervallo si rivela cruciale per ottenere dati dettagliati tramite la biopsia liquida. Di conseguenza, è essenziale che futuri studi clinico-traslazionali includano la ri-caratterizzazione molecolare del tumore in questo intervallo.
Un promettente sviluppo futuro è l’integrazione di approcci multimodali in studi clinici, combinando la biopsia liquida con metodiche avanzate come la trascrittomica, la proteomica e l’intelligenza artificiale per monitorare dinamicamente la risposta alla terapia. Questi studi permetterebbero di sviluppare modelli predittivi personalizzati, migliorando significativamente l’accuratezza delle decisioni cliniche.
Il microambiente tumorale: una rete di interazioni complesse
La marcata aggressività, la tendenza a metastatizzare precocemente e l’elevata resistenza alle terapie osservate nel SCLC sono in parte imputabili alla complessità del microambiente tumorale (TME). Il TME è una struttura complessa e dinamica, caratterizzata dalla presenza di cellule tumorali, immunitarie e stromali, nonché da una varietà di citochine e metaboliti. Questi componenti interconnessi possono sia potenziare la risposta immunitaria sia favorire la resistenza del tumore, riflettendo l’interdipendenza e la complessità delle interazioni biologiche all’interno del TME.14
Il TME del SCLC si presenta come una struttura complessa ed eterogenea, caratterizzata da interazioni dinamiche tra le cellule immunitarie e tumorali che possono promuovere o inibire la crescita e la progressione del tumore. Queste interazioni rivestono un ruolo cruciale, influenzando sia la patogenesi del tumore sia la sua capacità di resistere alle terapie convenzionali e immunoterapiche.15 È di estrema importanza, dunque, una più profonda comprensione delle dinamiche tra il sistema immunitario e il TME per migliorare l’efficacia delle strategie terapeutiche.
Il paradigma centrale dell’immunoterapia, che sfrutta la modulazione dell’asse PD-1/PD-L1, si fonda sulla capacità di questa interazione di regolare negativamente l’attività dei linfociti T, facilitando così l’escape immunitario del tumore (figura 3).16 L’impiego di anticorpi anti-PD-L1 non solo blocca questa interazione a livello tumorale, ma amplifica anche l’effetto immunomodulante nel sistema linfonodale, migliorando la presentazione dell’antigene e il priming dei linfociti T, con l’obiettivo di portare nuovi linfociti clonali nella zona del tumore.17 L’efficacia di tale strategia è influenzata dall’evoluzione tumorale e dalla comparsa di neoantigeni clonali.
FIGURA 3. Il ciclo dell’interazione tra immunità e tumore nel SCLC (figura tradotta da Chen et al. 2023).14
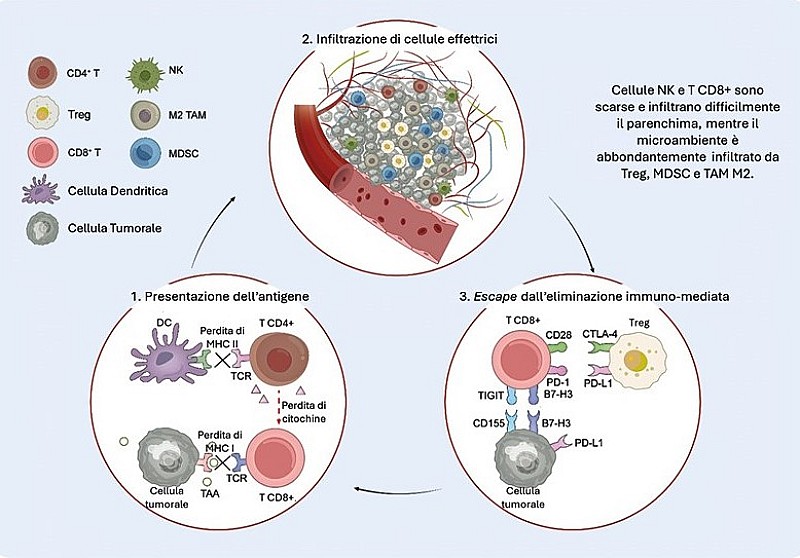
La suscettibilità dell’SCLC all’immunoterapia dipende inoltre dalla tipologia di cellule immunitarie presenti nell’infiltrato tumorale e dalle caratteristiche immunogeniche del TME. In particolare, tra i sottotipi di SCLC, quello “inflamed”, caratterizzato da un gene signature di tipo infiammatorio, ha mostrato di beneficiare maggiormente dell’aggiunta dell’immunoterapia alla chemioterapia (figura 4).18
FIGURA 4. Confronto delle caratteristiche del microambiente tumorale nei sottotipi di SCLC inflamed e noninflamed (modificata da Caliman et al. 2023).20
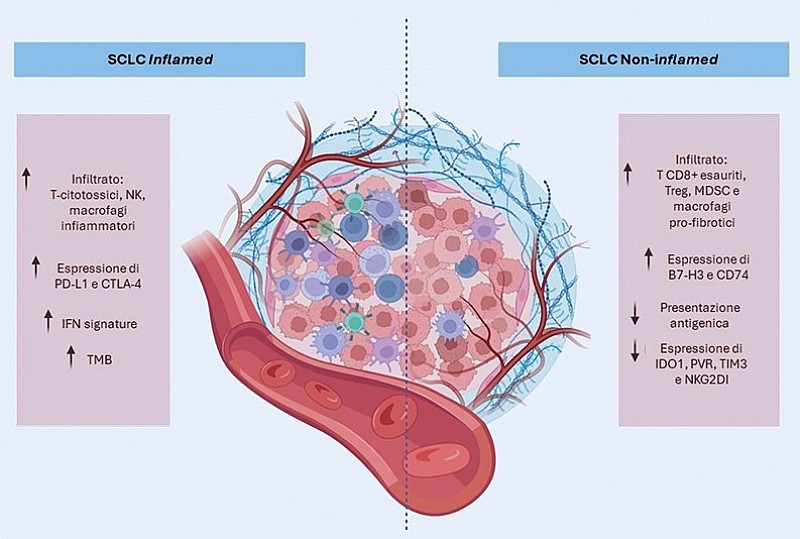
È stato notato inoltre che la lungo-sopravvivenza dei pazienti affetti da microcitoma correla con la presenza di cellule immunitarie nel TME.19 Pazienti lungo-sopravviventi presentano un rapporto inferiore di cellule immunitarie soppressive (come monociti, Treg e macrofagi) rispetto ai linfociti CD3+, mentre la presenza nell’infiltrato tumorale di elevati livelli di cellule Treg e cellule soppressori mieloidi circolanti (MDSCs), che possono inibire l’attivazione, l’espansione e le funzioni delle cellule T effettrici, correlano negativamente con gli esiti clinici.20
Per comprendere il ruolo del TME sulla crescita del SCLC e sulla risposta al trattamento, è cruciale condurre un’analisi approfondita delle interazioni tra i suoi componenti. È essenziale valutare non solo gli aspetti quantitativi ma anche quelli qualitativi di questi elementi. Inoltre, la variabilità individuale nell’equilibrio tra questi componenti è un fattore critico che può influenzare significativamente l’efficacia del trattamento.
L’analisi del TME dovrebbe essere condotta direttamente sui campioni di tessuto tumorale; tuttavia, l’attuazione di questo approccio è impraticabile nel contesto del SCLC. Pertanto, identificare biomarcatori surrogati nel sangue periferico che possano riflettere le dinamiche del TME rappresenta una sfida per la ricerca sul SCLC. Superare questa sfida non solo amplierebbe le possibilità di monitoraggio non invasivo, ma faciliterebbe anche l’applicazione di trattamenti personalizzati su larga scala. L’immunoterapia è infatti una strategia terapeutica complessa e dinamica e lo studio delle interconnessioni tra gli elementi immunitari e quelli tumorali sul singolo paziente consentirebbe di adottare strategie terapeutiche altamente personalizzate. In quest’ottica è essenziale ridefinire il concetto di “risposta” alla terapia, estendendolo oltre la tradizionale “risposta del tumore” per includere l’analisi della “risposta immunologica” inducibile dal tumore e dalla terapia stessa.
Non solo l’immunoterapia è in grado di interferire con l’immunità pro-tumorale, ma anche la chemioterapia ha dimostrato un effetto immunomodulante.21 È stato osservato che le dosi di chemioterapia in grado di modulare la risposta immunitaria sono generalmente inferiori a quelle necessarie per ottenere un effetto citotossico.21 Questa osservazione suggerisce la possibilità di rivedere le modalità di impiego della chemioterapia nei protocolli degli studi clinici, considerando il suo potenziale di modulazione del sistema immunitario. Adottare questi approcci integrati è essenziale per lo sviluppo di strategie terapeutiche che massimizzino il potenziale delle interazioni tra farmaci, tumore e sistema immunitario, ottimizzando così gli esiti per i pazienti.
Le prospettive future di ricerca clinica nel TME dell’SCLC includono la progettazione di studi clinici volti allo sviluppo di nuove terapie combinate che integrino l’immunoterapia con agenti modulatori del TME al fine di potenziare la risposta immunitaria antitumorale. Questi studi potrebbero allo stesso tempo sfruttare tecnologie come il single-cell RNA sequencing e la spettrometria di massa per mappare con precisione le interazioni cellulari nel TME durante la terapia. Tali approcci offrirebbero nuove opportunità per interventi terapeutici mirati e personalizzati, migliorando significativamente l’efficacia dei trattamenti.
Nuove strategie terapeutiche
L’introduzione dell’immunoterapia nell’armamentario terapeutico contro il microcitoma ha notevolmente migliorato la prognosi dei pazienti, i quali per trent’anni non hanno avuto a disposizione opzioni terapeutiche più efficaci.5,6,22,23 Nonostante ciò, l’immunoterapia offre un beneficio significativo solo per un gruppo ristretto di pazienti affetti da microcitoma.7 Questo sottolinea la necessità di una più profonda comprensione della complessità biologica della risposta al trattamento immunologico. Identificare biomarcatori predittivi e vulnerabilità terapeutiche differenziali è fondamentale per identificare i pazienti più propensi a ottenere un esito migliore e sviluppare approcci terapeutici personalizzati.
È importante considerare numerosi aspetti oltre alla notevole capacità antigenica del microcitoma e alla sua elevata probabilità di immunosensibilità.24,25 I soli biomarcatori immunitari classici, come PD-L1 e il TMB, non sembrano correlare con gli esiti clinici del trattamento chemio-immunoterapico.7
Le analisi trascrittomiche hanno consentito di mettere in evidenza la diversità molecolare tra i SCLC e svariati studi hanno tentato di correlare i sottotipi trascrittomici del SCLC con classificazioni immunoistochimiche più semplici; tuttavia, la variabilità inter- e intra- tumorale rimane un aspetto molto complesso.3,18,26-28
La più ampia analisi genomica condotta finora sul SCLC (3600 campioni tumorali), ha svelato aspetti cruciali della patobiologia di questo tumore. Tra questi, l’arricchimento di alcune alterazioni geniche, come quelle nel pathway p53/RB1, e la mutazione di geni, come STK11, che si associano ad aspetti prognostici di particolare interesse.29 Mentre la comprensione delle caratteristiche omiche e molecolari del SCLC continua a progredire, sarebbe particolarmente interessante lo sviluppo di studi prospettici che utilizzino i sottotipi tumorali come criteri di stratificazione. Tali studi consentirebbero di determinare con chiarezza l’efficacia dell’immunoterapia nei vari sottogruppi di SCLC.
L’innovazione nella ricerca terapeutica per il SCLC è orientata verso l’identificazione e l’esplorazione di diversi bersagli molecolari, integrando spesso queste strategie con l’immunoterapia. Gli sforzi attuali si concentrano principalmente sui fattori che influenzano il ciclo cellulare e i meccanismi di riparo del DNA, come gli inibitori di PARP (PARPi), sui modulatori epigenetici (EZH2 e LSD1) e sulle vie di segnalazione come quella di NOTCH e DLL3.30 31 In questo contesto anche le terapie anti-angiogeniche, che fino a poco tempo fa hanno ottenuto scarsi risultati clinici nel SCLC, stanno emergendo come un’area di interesse su cui concentrare l’attenzione per lo sviluppo di nuove strategie terapeutiche.32
Gli approcci terapeutici che combinano farmaci mirati a diversi meccanismi molecolari/cellulari non solo cercano di arrestare la progressione tumorale, ma puntano anche a sensibilizzare le cellule tumorali ai trattamenti già esistenti. In questo contesto, l’avanzamento della ricerca clinica nel campo dell’SCLC include lo sviluppo di studi che combinino immunoterapia con agenti terapeutici diretti contro specifici target molecolari identificati attraverso analisi genomiche ed epigenomiche.
Conclusioni
Il trattamento del SCLC si sta orientando verso un approccio sempre più personalizzato che fonde una profonda comprensione delle dinamiche molecolari e immunologiche della malattia con l’adozione di strategie terapeutiche innovative. L’impiego dell’immunoterapia e di trattamenti mirati, sostenuto da dati emergenti, sta infondendo nuove speranze per i pazienti affetti da SCLC. Tuttavia, il successo di questi avanzamenti terapeutici dipende dalla capacità di adattare e applicare queste strategie in modo personalizzato, rispondendo alle specificità di ogni singolo tumore e paziente.
Tra le prospettive di ricerca più interessanti vi è l’integrazione, nei futuri studi clinici, di tecnologie innovative, come la biopsia liquida e la mappatura dettagliata delle interazioni cellulari nel microambiente tumorale. Inoltre, la sperimentazione di terapie combinate basate sul profilo genetico e molecolare specifico del tumore in vari stadi della sua evoluzione potrebbe portare all’individuazione di trattamenti più efficaci e mirati.
La stretta collaborazione tra la ricerca traslazionale e quella clinica sarà fondamentale per tradurre le scoperte scientifiche in miglioramenti concreti per i pazienti, aprendo la strada a trattamenti veramente personalizzati per il SCLC. L’accesso a coorti di pazienti più ampie e lo sviluppo di progetti di collaborazione su scala nazionale e internazionale saranno cruciali per validare queste nuove strategie e implementarle nella pratica clinica.
Se queste prospettive si concretizzeranno, contribuiranno a far progredire la rivoluzione terapeutica già avviata con l’introduzione dell’immunoterapia nel trattamento del SCLC, fornendo ulteriori opzioni terapeutiche e strumenti clinici per combattere questa devastante patologia, offrendo una speranza concreta ai pazienti.
Referenze
1. Gazdar AF, Bunn PA, Minna JD. Small-cell lung cancer: what we know, what we need to know and the path forward. Nat Rev Cancer 2017;17(12):725-37.
2. Schwendenwein A, Megyesfalvi Z, Barany N, et al. Molecular profiles of small cell lung cancer subtypes: therapeutic implications. Mol Ther On-colytics 2021;20:470-83.
3. Rudin CM, Brambilla E, Faivre-Finn C, et al. Small-cell lung cancer. Nat Rev Dis Primers 2021;7(1):3.
4. Solta A, Ernhofer B, Boettiger K, et al. Small cells - big issues: biological implications and preclinical advancements in small cell lung cancer. Mol Cancer 2024;23(1):41.
5. Horn L, Mansfield AS, Szczesna A, et al. First-Line Atezolizumab plus Chemotherapy in Extensive-Stage Small-Cell Lung Cancer. N Engl J Med 2018;379(23):2220-29.
6. Goldman JW, Dvorkin M, Chen Y, et al. Durvalumab, with or without tremelimumab, plus platinum-etoposide versus platinum-etoposide alone in first-line treatment of extensive-stage small-cell lung cancer (CASPIAN): updated results from a randomised, controlled, open-label, phase 3 trial. Lancet Oncol 2021;22(1):51-65.
7. Lorenzi M, Resi MV, Bonanno L, et al. Tissue and circulating biomarkers of benefit to immunotherapy in extensive-stage small cell lung cancer patients. Front Immunol 2024;15:1308109.
8. Zhang W, Xia W, Lv Z, et al. Liquid Biopsy for Cancer: Circulating Tumor Cells, Circulating Free DNA or Exosomes? Cell Physiol Biochem 2017;41(2):755-68.
9. Aggarwal C, Wang X, Ranganathan A, et al. Circulating tumor cells as a predictive biomarker in patients with small cell lung cancer undergoing chemotherapy. Lung Cancer 2017;112:118-25.
10. Hamilton G, Rath B, Stickler S. Significance of circulating tumor cells in lung cancer: a narrative review. Transl Lung Cancer Res 2023;12(4):877-94.
11. Almodovar K, Iams WT, Meador CB, et al. Longitudinal Cell-Free DNA Analysis in Patients with Small Cell Lung Cancer Reveals Dynamic Insights into Treatment Efficacy and Disease Relapse. J Thorac Oncol 2018;13(1):112-23.
12. Nong J, Gong Y, Guan Y, et al. Circulating tumor DNA analysis depicts subclonal architecture and genomic evolution of small cell lung cancer. Nat Commun 2018;9(1):3114.
13. Mohan S, Foy V, Ayub M, et al. Profiling of Circulating Free DNA Using Targeted and Genome-wide Sequencing in Patients with SCLC. J Thorac Oncol 2020;15(2):216-30.
14. Chen Y, Li H, Fan Y. Shaping the tumor immune microenvironment of SCLC: Mechanisms, and opportunities for immunotherapy. Cancer Treat Rev 2023;120:102606.
15. Dutta R, Rathor A, Sharma HP, et al. Mapping the immune landscape in small cell lung cancer by analysing expression of immuno-modulators in tissue biopsies and paired blood samples. Sci Rep 2023;13(1):3739.
16. Meng L, Wu H, Wu J, et al. Mechanisms of immune checkpoint inhibitors: insights into the regulation of circular RNAS involved in cancer hall-marks. Cell Death Dis 2024;15(1):3.
17. Fransen MF, Schoonderwoerd M, Knopf P, et al. Tumor-draining lymph nodes are pivotal in PD-1/PD-L1 checkpoint therapy. JCI Insight 2018 Dec 6;3(23):e124507.
18. Gay CM, Stewart CA, Park EM, et al. Patterns of transcription factor programs and immune pathway activation define four major subtypes of SCLC with distinct therapeutic vulnerabilities. Cancer Cell 2021;39(3):346-60 e7.
19. Muppa P, Parrilha Terra SBS, Sharma A, et al. Immune Cell Infiltration May Be a Key Determinant of Long-Term Survival in Small Cell Lung Cancer. J Thorac Oncol 2019;14(7):1286-95.
20. Caliman E, Fancelli S, Petroni G, et al. Challenges in the treatment of small cell lung cancer in the era of immunotherapy and molecular classifi-cation. Lung Cancer 2023;175:88-100.
21. Mukherjee O, Rakshit S, Shanmugam G, et al. Role of chemotherapeutic drugs in immunomodulation of cancer. Curr Res Immunol 2023;4:100068.
22. Remon J, Hendriks LEL, Mountzios G, et al. MET alterations in NSCLC-Current Perspectives and Future Challenges. J Thorac Oncol 2023;18(4):419-35.
23. Liu SV, Reck M, Mansfield AS, et al. Updated Overall Survival and PD-L1 Subgroup Analysis of Patients With Extensive-Stage Small-Cell Lung Can-cer Treated With Atezolizumab, Carboplatin, and Etoposide (IMpower133). J Clin Oncol 2021;39(6):619-30.
24. Alexandrov LB, Nik-Zainal S, Wedge DC, et al. Signatures of mutational processes in human cancer. Nature 2013;500(7463):415-21.
25. Mahadevan NR, Knelson EH, Wolff JO, et al. Intrinsic Immunogenicity of Small Cell Lung Carcinoma Revealed by Its Cellular Plasticity. Cancer Di-scov 2021;11(8):1952-69.
26. Lissa D, Takahashi N, Desai P, et al. Heterogeneity of neuroendocrine transcriptional states in metastatic small cell lung cancers and pa-tient-derived models. Nat Commun 2022;13(1):2023.
27. Baine MK, Hsieh MS, Lai WV, et al. SCLC Subtypes Defined by ASCL1, NEUROD1, POU2F3, and YAP1: A Comprehensive Immunohistochemical and Histopathologic Characterization. J Thorac Oncol 2020;15(12):1823-35.
28. Rudin CM, Poirier JT, Byers LA, et al. Molecular subtypes of small cell lung cancer: a synthesis of human and mouse model data. Nat Rev Cancer 2019;19(5):289-97.
29. Sivakumar S, Moore JA, Montesion M, et al. Integrative Analysis of a Large Real-World Cohort of Small Cell Lung Cancer Identifies Distinct Ge-netic Subtypes and Insights into Histologic Transformation. Cancer Discov 2023;13(7):1572-91.
30. Poirier JT, George J, Owonikoko TK, et al. New Approaches to SCLC Therapy: From the Laboratory to the Clinic. J Thorac Oncol 2020;15(4):520-40.
31. Grenda A, Krawczyk P, Obara A, et al. Transitioning to a Personalized Approach in Molecularly Subtyped Small-Cell Lung Cancer (SCLC). Int J Mol Sci 2024 Apr 10;25(8):4208.
32. Cani M, Napoli VM, Garbo E, et al. Targeted Therapies in Small Cell Lung Cancer: From Old Failures to Novel Therapeutic Strategies. Int J Mol Sci 2023 May 17;24(10):8883.















 Eurosets presenta Landing Advance, un sistema completo e intuitivo che apre nuove frontiere nel campo del monitoraggio multiparametrico in cardiochirurgia...
Eurosets presenta Landing Advance, un sistema completo e intuitivo che apre nuove frontiere nel campo del monitoraggio multiparametrico in cardiochirurgia...






