Professione medica
Endocrinologia
21/10/2025
I parametri modificabili nei sistemi automatizzati di erogazione di insulina
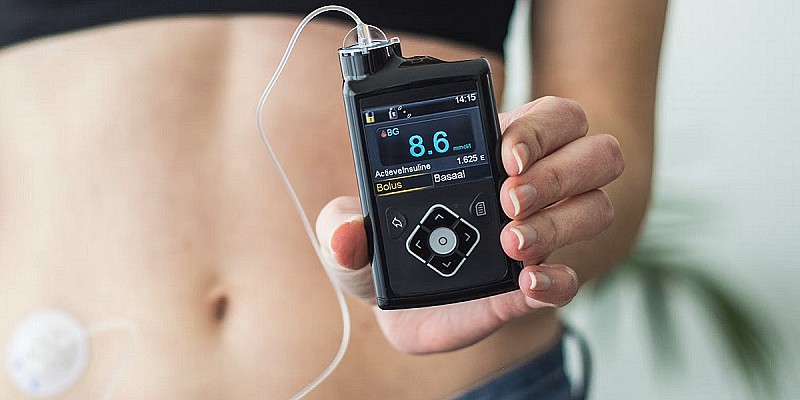
I sistemi per la somministrazione automatizzata di insulina modulano automaticamente l’erogazione insulinica in base ai valori glicemici rilevati in continuo da un sensore, tramite sofisticati algoritmi di controllo
Il diabete mellito di tipo 1 (DM1) colpisce circa 300 000 pazienti in Italia, con una prevalenza pari allo 0.5% della popolazione generale, rappresentando circa il 5–10% di tutti i casi di diabete. Si tratta di una patologia cronica su base autoimmune, che comporta un deficit insulinico assoluto e richiede la somministrazione esogena di insulina per tutta la vita.
La terapia insulinica convenzionale si basa su uno schema basal-bolus, che prevede la somministrazione di insuline basali a lunga durata d’azione per mimare la secrezione endogena continua, e di insuline prandiali ad azione rapida o ultra-rapida prima di ogni pasto. Tuttavia, è ampiamente dimostrato che il fabbisogno insulinico giornaliero presenta un’elevata variabilità, sia inter-individuale che intra-individuale.
In questo contesto si inseriscono i sistemi per la somministrazione automatizzata di insulina (AID, Automated Insulin Delivery), che modulano automaticamente l’erogazione insulinica in base ai valori glicemici rilevati in continuo da un sensore, tramite sofisticati algoritmi di controllo.
Numerosi studi clinici hanno dimostrato la superiorità di tutti i sistemi AID attualmente in commercio rispetto alla terapia convenzionale nel migliorare i parametri glicemici e ridurre il rischio ipoglicemico, consentendo ai pazienti di raggiungere più facilmente gli obiettivi raccomandati dalle linee guida internazionali. Per tale motivo, i sistemi AID rappresentano oggi il gold standard per il trattamento insulinico nel DM1.
I dispositivi attualmente disponibili in commercio offrono numerose possibilità di personalizzazione, grazie a parametri specifici di impostazione, alcuni comuni alla maggior parte dei sistemi, altri peculiari per ciascun dispositivo. Conoscere e gestire correttamente questi parametri rappresenta un passo cruciale per ottimizzare la terapia insulinica e personalizzarla ulteriormente, migliorando l’efficacia, la sicurezza e l’aderenza terapeutica.
I sistemi AID richiedono il collegamento a un sensore glicemico in continuo (CGM, Continuous Glucose Monitoring) e l’impostazione iniziale di alcuni parametri per permettere al sistema di avviare il meccanismo di erogazione automatica dell’insulina, controllato dal proprio algoritmo. Alcuni di questi parametri possono essere modificati nel tempo durante il follow-up, per garantire una terapia sempre più personalizzata e aderente alle esigenze glicemiche del paziente: è quindi essenziale che il clinico abbia una conoscenza approfondita dei parametri di avvio e di quelli modificabili per ogni sistema, al fine di gestire al meglio la terapia.
Sul sito AME sono oggi disponibili i dettagli relativi ai metodi di stima e le relative implicazioni cliniche.
Questi sono i principali parametri impostabili manualmente nei sistemi (A)HCL (-Advanced-, Hybrid Closed Loop):
• calcolo della dose insulinica totale (TDD, Total Daily Dose) e velocità della basale;
• rapporto insulina/carboidrati (I:CHO);
• fattore di sensibilità insulinica (FSI);
• tempo di insulina attiva (AIT – Active Insulin Time);
• insulin on board (IOB) o bolus on board (BOB);
• target glicemico.
Bibliografia
1. Dovc K, Boughton C, Tauschmann M, et al. Young children have higher variability of insulin requirements: observations during hybrid closed-loop insulin delivery. Diabetes Care 2019, 42: 1344–7.
2. Diabetes Technology: Standards of Care in Diabetes—2025. Diabetes Care 2025, 48 suppl 1: S146–66.
3. Di Molfetta S, Rossi A, Assaloni R, et al. Tips for successful use of commercial automated insulin delivery systems: an expert paper of the Italian working group on diabetes and technology. Diabetes Res Clin Pract 2025, 223: 112117.
4. Phillip M, Nimri R, Bergenstal RM. Consensus recommendations for the use of automated insulin delivery technologies in clinical practice. Endocr Rev 2023, 44: 254-80.
5. Castañeda J, Arrieta A, Van den Heuvel T, et al. Time in tight glucose range in type 1 diabetes: predictive factors and achievable targets in real-world users of the MiniMed 780G system. Diabetes Care 2024, 47: 790-7.
6. Messer LH, Breton MD. Therapy settings associated with optimal outcomes for t:slim X2 with Control-IQ Technology in real-world clinical care. Diabetes Technol Ther 2023, 25: 877-82.
7. Forlenza GP, DeSalvo DJ, Aleppo G. Real-world evidence of Omnipod® 5 automated insulin delivery system use in 69,902 people with type 1 diabetes. Diabetes Technol Ther 2024, 26: 514-25.
Se l'articolo ti è piaciuto rimani in contatto con noi sui
nostri canali social seguendoci su:
nostri canali social seguendoci su:
Oppure rimani sempre aggiornato in ambito farmaceutico iscrivendoti alla nostra Newsletter!
POTREBBERO INTERESSARTI ANCHE
Il 25,7% degli ultrasessantenni può sospendere la LT4 mantenendo funzione tiroidea adeguata a un anno, un editoriale indica anche le soglie di TSH da considerare nella pratica
In occasione della Giornata Mondiale degli Ormoni, AME raccomanda un approccio diagnostico integrato
La SIO richiama uno studio su UK Biobank: l’assenza iniziale di diabete o ipertensione non esclude un aumento del rischio cardiaco ed epatico nelle persone con obesità















 Eurosets presenta Landing Advance, un sistema completo e intuitivo che apre nuove frontiere nel campo del monitoraggio multiparametrico in cardiochirurgia...
Eurosets presenta Landing Advance, un sistema completo e intuitivo che apre nuove frontiere nel campo del monitoraggio multiparametrico in cardiochirurgia...






